|
||||||||||||||||||||||||||||||||||||||||||
![]()
|
L'air est un mélange
Ce mélange qui
constitue l'atmosphère terrestre, n'existe nulle part ailleurs dans le système solaire. En 1895, procédé de liquéfaction de
l'air dû à Carl von Linde (1842-1934). |
Un des quatre de l'Antiquité: terre, air, eau et feu. |
|
|
||||||||||||||||||||||||||||||
|
Il est continuellement recyclé
par les bactéries qui se nourrissent des déchets végétaux et animaux.
Les animaux l'absorbent pour
respirer et alimenter la combustion interne. Les végétaux en produisent par
photosynthèse grâce à l'énergie solaire. |
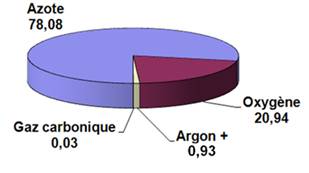
Composition
de l'air sec en %
|
|||||||||||||||||||||||||||||
|
La photosynthèse des végétaux
l'absorbe.
et quelques traces d'ozone, de krypton et xénon.
Éléments dont le pourcentage est
fixe: azote, oxygène, argon, néon, hélium et krypton; Éléments dont le pourcentage est
variable avec le lieu et la période:
dioxyde de carbone, vapeur d'eau, méthane, dioxyde de sulfure, ozone, oxydes
nitriques. |
||||||||||||||||||||||||||||||
Voir Oxygène / Azote / Dioxyde de carbone
|
|
|
|
Respiration humaine:
Masse volumique de l'air: 1, 2kg / m3.
|
|
Voir Mécanisme
de la respiration / Respiration
des plantes / Corps humain
|
Les
molécules de l'air (N2
et O2) se sont pas liées et n'ont pas d'interactions
(contrairement aux solides et aux liquides). Vitesse:
330 m/s à 25°C Collisions:
10 milliards de fois par seconde à température ambiante. Pression sur un autre corps (parois du récipient par
exemple): force exercée par les molécules qui se cognent sur chaque unité de
surface. La quantité de collision détermine la température. Avec la même
quantité de molécules dans le même volume, en abaissant la température, les
molécules ralentissent; moins de collisions; la pression diminue. |
|
|
À
chaque respiration, chacun d'entre nous est susceptible d'inhaler 50 millions
de molécules d'air expirées par Léonard de Vinci à un moment ou un autre.
C'est aussi vrai pour toute personne ayant vécu 65 ans et dont la respiration
aurait été répartie uniformément à travers l'atmosphère.
Quant au dernier soupir de Jules César, vous pouvez compter en inhaler
environ six molécules. |
At every breath, each of us is likely to inhale some
50 million molecules of air exhaled at some time by Leonardo da Vinci or, for
that matter, by any person who lived for
65 years and whose breath has been well distributed throughout the
atmosphere. Of Julius Caesar's dying breath, you can expect to inhale about
six molecules. Curious and Interesting Mathematics – David Wells –
Penguin book - 1997 |
Voir Molécules d'eau du bain
d'Archimède
Poids de l'air
|
Demandez s'il est possible de porter à bout de bras le poids de l'air d'une pièce normale. Il sera étonné de
savoir que c'est impossible. Exemple:
Pièce de 4 m x 4 m et
3 m de haut: 48 m3. Masse volumique de l'air: 1,2 kg/m3 au niveau de la mer à 20
°C. Poids de l'air dans la pièce: 57,6 kg. |
|
Les molécules du gaz de l'air occupent moins de 0,1 % de
l'espace; le reste c'est rien. On trouve environ 26 trillions de molécules dans 1 cm3
(26 x 1018). La pression atmosphérique est égale à environ 1 bar, ce qui
correspond à un poids de 10 000 kg par mètre carré. Notre tête supporte une
pression de l'atmosphère d'environ 1000 kg (1 tonne). Nous sommes composés de molécules qui exercent une pression
vers l'extérieur qui est pratiquement aussi élevée que la pression
atmosphérique. |
![]()
|
Voir |
|
|
Aussi |
|
|
Livres |
|
|
Sites |
|
|
Cette page |
![]()